 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
电池PtIH2(101.325kPa)IHCl(0.10mol Kg^-1)lHg2Cl2(s)IHg电动势E与温度T的关系为:
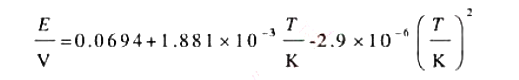
(1)写出电池反应:
(2)计算25℃时该反应的∆r G_m、∆r 〖SG〗_m、∆r 〖GH〗m以及电池恒温可逆放电时该反应过程的Qrm。
(3)若反应在电池外在同样条件恒压进行,计算系统与环境交换的热。
 更多“电池PtIH2(101.325kPa)IHCl(0.10mol Kg^-1)lHg2Cl2(s)IHg电动势E与温度T的关系为: (1)写出电”相关的问题
更多“电池PtIH2(101.325kPa)IHCl(0.10mol Kg^-1)lHg2Cl2(s)IHg电动势E与温度T的关系为: (1)写出电”相关的问题
第1题
电池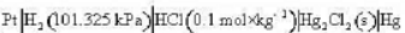 电动势召与温度T的关系为
电动势召与温度T的关系为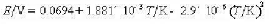
(1)写出电池反应:(2)计算25°C时该反应的DrCm.DrSm.DrHm以及电池恒温可逆放电时该反应过程的Qr.m
第2题
-4(T/K一298).试计算在298K,当电池有2mol电子的电量通过时,电池反应的 和此过程的可逆热效应
和此过程的可逆热效应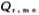
第3题
电池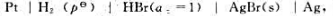 请:
请:
(1)写出电极反应与电池反应:
(2)若电池的电动势E/V=0.07131-4.99×10-6×(T/K-298),求正极在298K时的标准电极电势Eθ及电池反应的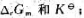
(3)判断此电池在298K时吸热还是放热,为什么?
(4)若HBr的浓度b=0.1mol·kg-1,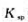 =1.00×10-12,电极Eθ(Ag+IAg)=0.80V,求电池的标准电动势Eθ.
=1.00×10-12,电极Eθ(Ag+IAg)=0.80V,求电池的标准电动势Eθ.
第4题
298K时,电池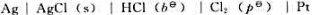 的电动势为1.1362v,电动势的温度系数为-5.95X10-4V·K-1.
的电动势为1.1362v,电动势的温度系数为-5.95X10-4V·K-1.
(1)写出电池反应;
(2)计算298K时该反应的 和标准平衡常数
和标准平衡常数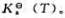
第5题
,E^θ(CIlAgCIlAg)=0.2222V,电池电动势的温度系数为:
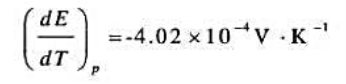
(1)写出电池反应;
(2)计算反应的标准平衡常数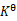 ;
;
(3)计算电池反应的可逆热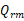 ;
;
(4)求溶液中ZnCl2的平均离子活度因子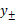 。
。
第6题
IZn)=-0.7620V.E-[CI-IAgCl(s)IAgI=0.2222V.电池电动势的温度系数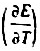 =-4.02x10-4V·K-1.
=-4.02x10-4V·K-1.
(1)写出电池反应;
(2)计算反应的标准平衡常数Kθ;
(3)计算电池反应可逆热Qr,m;
(4)求溶液中ZnCl2的平均离子活度因子ya.
第7题
t(s)的电动势E=-1.228V,H2O(l)的标准生成焰为-285.5kJ·mol-1,请:
(1)写出电极反应及电池反应;
(2)求该电池的电动势温度系数;
(3)求电池反应的 ;
;
(4)求273K时电池的电动势(假设反应热ΔtHmθ在0~25C之间不随温度变化).
第8题
298K时,下列电池的电动势为1.228V:
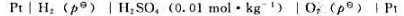
已知H2O(I)的标准生成焓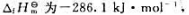 试求:
试求:
(1)该电池的温度系数:
(2)该电池在273K时的电动势.设反应焓在273~298K间为常数.
第9题
电池Ag(s)AgCl(s)]KCl(m)|Hg2Cl2(s)|HIg(I)的电池反应为
Ag(s)+1/2Hg2CI2(s)→AgCl(s)+Hg(I),已知298K时,此电池反应的焓变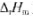 为5435/mol,各物质的规定熵数据为
为5435/mol,各物质的规定熵数据为
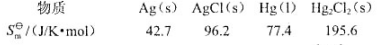 试计算该温度下电池的电动势E及电池电动势的温度系数
试计算该温度下电池的电动势E及电池电动势的温度系数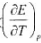
第10题
在一定的温度下,为使电池
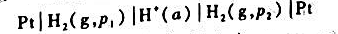
的电动势E为正值,则必须使氢电极中H2(g)的分压p1()p2.(填>,<,=.)

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
