 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
IZn)=-0.7620V.E-[CI-IAgCl(s)IAgI=0.2222V.电池电动势的温度系数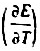 =-4.02x10-4V·K-1.
=-4.02x10-4V·K-1.
(1)写出电池反应;
(2)计算反应的标准平衡常数Kθ;
(3)计算电池反应可逆热Qr,m;
(4)求溶液中ZnCl2的平均离子活度因子ya.
 更多“25°C时.电池ZnIZnCl2(0.55mol.Kg-1)IAgCl(s)IAg的电动势E=1.015V.已知E(Zn2+”相关的问题
更多“25°C时.电池ZnIZnCl2(0.55mol.Kg-1)IAgCl(s)IAg的电动势E=1.015V.已知E(Zn2+”相关的问题
第1题
25℃时测得下列电池的电动势为0.622V,求配合物Ag(CN)2-的稳定常数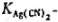 。(已知
。(已知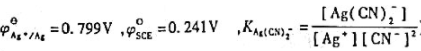 )
)
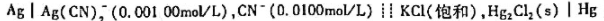
第2题
计算25°C时,下列电池的电动势,并标明电池的正负极。
已知:
Ag,AgCl|NaCl(0.1mol•L^-1),NaF(0.001mol•L^-1)1LaFs单晶膜
|NaF(0.1mol•L^-1)|ISCE
第3题
,E^θ(CIlAgCIlAg)=0.2222V,电池电动势的温度系数为:
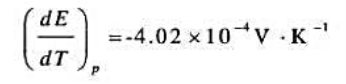
(1)写出电池反应;
(2)计算反应的标准平衡常数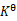 ;
;
(3)计算电池反应的可逆热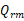 ;
;
(4)求溶液中ZnCl2的平均离子活度因子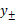 。
。
第4题
994V。
(1)写出电极反应和电池反应:
(2)25℃时实验测得H2SO4浓度为b时,上述电池的电动势为0.623V。已知此H2SO4溶液的离子平均活度因子y±=0.7,求b为多少;
(3)计算Ag2SO4(s)的活度积Ksp^θ。
第5题
电池: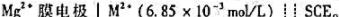 。在25℃时,测得电动势为0.387V。
。在25℃时,测得电动势为0.387V。
(1)当用未知溶液代替上述已知Mg2+溶液时。测得电池电动势为0.425V,求此溶液的pMg为多大?
(2)若溶液替代引起液接电位Ej的不稳定值为±1mV,则Mg2+浓度测定产生的相对误差有多大?波动范围为多少?
第6题
25℃时,电池Pt|H2(pθ)|H2SO4(a=1)IAu3O3,Au的电动势E=I.362V.请:
(1)写出电极反应和电池反应:
(2)25℃时电池的标准电动势和反应的ΔtGm及Kθ;
(3)25℃时Au2O3的标准生成摩尔吉布斯丽数:
(4)25℃时Au与Au2O3平衡时O2的活度和压强.
已知H2O(l)的标准生成青布斯兩数ΔtGmθ(298K)=-236kJ·mol-1.
第7题
标准生成摩尔吉布斯丽数和标准摩尔反应始分别为-237.2kJ·mol-1和-285.85kJ·mol-1,请:
(1)写出电极反应和电池反应:
(2)求电池的标准电动势和反应的ΔtGmθ;
(3)求25℃时,下列反应的ΔtGmθ及氧气的分压:2HgO(=2Hg+O2);
(4)求反应H2(pθ)+-½(pθ)=H2O(l)的ΔtSmθ和反应热.
第9题
甲烷燃烧过程可设计成燃料电池.当电解质为酸性溶液时,电极反应和电池反应分别为
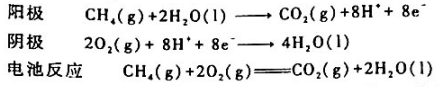
已知,25°C时有关物质的标准摩尔生成吉布斯函数 为
为
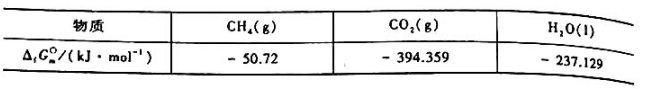
计算25°C时该电池的标准电动势.
第10题
已知铅酸蓄电池
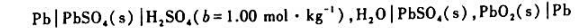
在25°C时的电动势E=1.9283V,Eθ=2.0501V.该电池的电池反应为
Pb(s)+PbO2(s)+2SO42-+4H+→2PbSO4(s)+2H2O
(1)请写出该电池的电极反应;
(2)计算该电池中硫酸溶液的活度a、平均离子活度az及平均离子活度因子γz;
(3) 已知该电池的温度系数为5.664x10-5V·K-1,计算电池反应的ΔrGm,ΔrSm,ΔrHm,
及可逆热Qr,m.

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
