 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 更多“已知钠的原子化焓为108.7kJ·mol-1,第一和第二电离能分别为494kJ·mol-1和4560kJ·mo”相关的问题
更多“已知钠的原子化焓为108.7kJ·mol-1,第一和第二电离能分别为494kJ·mol-1和4560kJ·mo”相关的问题
第1题
已知钡的升华焓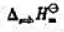 =180.0kJ·mol-1,第一、第二电离能分别为
=180.0kJ·mol-1,第一、第二电离能分别为
507.94kJ·mol-1和971.44kJ·mol-1,Ba2+(aq)的标准摩尔生成烩的相对值(Ba2+,q)=-537.64kJ.mol-1.试用热力学循环计算;(1)Ba2+(g)的标准摩尔生成焓ΔlHθm(Ba2+,g);(2)Ba2+(g)的水合焓ΔhHθm(Ba2+,g).
第3题
解释下列现象:
(1)Na的第一电离能小于Mg,面Na的第二电离能却大大超过Mg.
(2)Na+和Ne是等电子体,为什么它们的第一电离能的数值差别较大?
(3)Be原子的第一、二、三、四各级电离能分别为899,1757,1.484×104和2.100×104kJ·mol-1,解释各级电离能逐渐增大并有突跃的原因.
第4题
根据下列已知数据,由玻恩-哈伯循环计算氯化钡的 。
。
氯分子的解离能 242.6 kJ·mol-1
钡的原子化热177.8 kJ·mol-1
钡的第一电离能550.9 kJ·mol-¿105 106¿
钡的第二电离能962.3 kJ·mol-1
氯的电子亲和能348.6 kJ·mol-1
氯化钡的晶格能2026.7 kJ·mol-1
第5题
(I)的标准摩尔生成焓分别为-394kJ·mol-1和-286kJ·mol-1计算C2H5OH(1)在298.15K时的标准摩尔生成焓。
第6题
A.首先第一和第二同时不超过目标值,然后第三目标不超过目标值。
B.第一、第二和第三目标同时不超过目标值。
C.第一和第二目标恰好达到目标值,第三目标不超过 目标值。
D.首先第一和第二同时不低于目标值,然后第三目标不低于目标值。
第7题
A.-227.6
B.227.6
C.385.3
D.-385.3
第8题
(I)为419.0kJ·mol-1,碘分子的解离能(D)为213.38 kJ·mol-1,碘的电子亲和能(E)为-295.0 kJ·mol-1,求碘化钾的标准摩尔生成焓。
第10题
已知298.15K时,CH3COOH(CO2(g)和H2O(1)的标准摩尔生成焓 分别为-487kJ·mol-1、-394kJ·mol-1和-286kJ·mol-1,则反应
分别为-487kJ·mol-1、-394kJ·mol-1和-286kJ·mol-1,则反应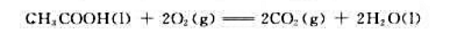 在298.15K时的标准摩尔焓变ΔH2为(),
在298.15K时的标准摩尔焓变ΔH2为(),
A、193kJ·mol-1
B、873kJ·mol-1
C、-193kJ·mol-1
D、-873kJ·mol-1

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
