 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
(I)的标准摩尔生成焓分别为-394kJ·mol-1和-286kJ·mol-1计算C2H5OH(1)在298.15K时的标准摩尔生成焓。
 更多“已知298.15K时C2H5OH(I)的标准摩尔燃烧焓为-1367kJ·mol-1CO2(g)和H2O”相关的问题
更多“已知298.15K时C2H5OH(I)的标准摩尔燃烧焓为-1367kJ·mol-1CO2(g)和H2O”相关的问题
第1题
A.A.-195kJ·mol-1
B.B.195kJ·mol-1
C.C.-875kJ·mol-1
D.D.875kJ·mol-1
第2题
已知25℃甲酸甲酯的标准摩尔燃烧焓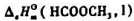 为-979.5kJ·mol-1,甲酸(HCOOH,I)、甲醇(CH3OH,1)、水(H2O,I)及二氧化碳(CO2,g)的标准摩尔生成焓
为-979.5kJ·mol-1,甲酸(HCOOH,I)、甲醇(CH3OH,1)、水(H2O,I)及二氧化碳(CO2,g)的标准摩尔生成焓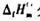 分别为-424.72kJ·mol-1,-238.66kJ·mol-1,-285.83kJ·mol-1及-393.509kJ·mol-1.应用这些数据求25℃时下列反应的标准摩尔反应焓.
分别为-424.72kJ·mol-1,-238.66kJ·mol-1,-285.83kJ·mol-1及-393.509kJ·mol-1.应用这些数据求25℃时下列反应的标准摩尔反应焓.

第3题
A.A. ΔtHmθ(T)是H2O(g)的标准摩尔生成焓.
B.B. ΔtHmθ(T)是H2O(g)的标准摩尔燃烧焓.
C.C. ΔtHmθ(T)是负值.
D.D. ΔtHmθ(T)与反应的ΔtUmθ(T)数值不相等.
第4题
反应Ag2O(s)+2HCl(g)——2AgCl(s)+H2O(1)在298.15K时的标准摩尔焓变
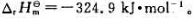 。已知298.15K时Ag2O(s)、HCl(g)和H2O的标准摩尔生成焓ΔH分别为-31.0kJ·mol-1、-92.3kJ·mol-1和-285.4kJ·mol-1,试计算298.15K时AgCl(s)的标准摩尔生成焓。
。已知298.15K时Ag2O(s)、HCl(g)和H2O的标准摩尔生成焓ΔH分别为-31.0kJ·mol-1、-92.3kJ·mol-1和-285.4kJ·mol-1,试计算298.15K时AgCl(s)的标准摩尔生成焓。
第5题
已知298.15 K时CH4(g) ,CO2(g),H2O(1)的标准摩尔生成焓 分别为-74.81 kJ·mol-1,-393.51 kJ·mol-1,-285.83 kJ·mol-1,则298.15 K时CH4(g)的标准摩尔燃烧焓
分别为-74.81 kJ·mol-1,-393.51 kJ·mol-1,-285.83 kJ·mol-1,则298.15 K时CH4(g)的标准摩尔燃烧焓
A. -890.36 kJ· mol-1
B. 890.36 kJ· mol-1
C. -604.53 kJ· mol-1
D.604.53 kJ· mol-1
第7题
A.-227.6
B.227.6
C.385.3
D.-385.3
第8题
kJ.mol^-1。计算在氢氧燃料电池中进行下列反应时电池的电动势及其温度系数,

(2)应用表7.7.1的数据计算上述电池的电动势。
第9题
生成焓;(2)N2H4的标准摩尔燃烧焓;(3)N2H4与N2O4反应生成N2(g)和H2O(I)的标准摩尔反应焓.已知:
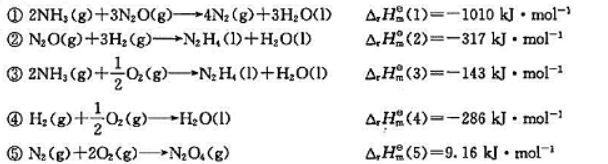
第10题
已知25C甲酸乙酯(HCOOCH3,1)的标准摩尔摩尔燃烧焓
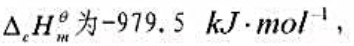
甲酸乙酯(HCOOCH3,1)、甲醇(CH3OH,1).水(H20,1)及二氧化碳(C02,g)的标准摩尔生成焓数据∆ƒH_m^θ分别为-424.72kJ.mol^-1,-238.66kJ.mol^-1,-285.83kJ.mol^-1及-393.509kJ.mol^-1。应用这些数据求25℃时下列反应的标准摩尔反应焓。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
