 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
锰元素在酸性介质中的元素标准电极电势图为
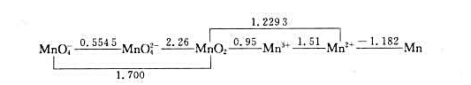
(1)试判断哪些物质可以发生歧化反应?写出歧化反应式;
(2)估计在酸性介质中,哪些物质是比较稳定的?
(3)试计算在酸性介质中电对MnO/Mn2+的标准电极电势。
 更多“锰元素在酸性介质中的元素标准电极电势图为 (1)试判断哪些物质可以发生歧化反应?写出歧化”相关的问题
更多“锰元素在酸性介质中的元素标准电极电势图为 (1)试判断哪些物质可以发生歧化反应?写出歧化”相关的问题
第1题
铬元素在酸性介质中的元素标准电极电势(ER/V)图为
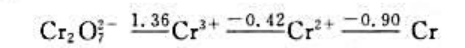
(1) 计算
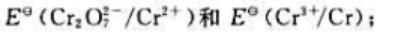
(2)判断Cr²+和Cr3+在酸性介质中是否发生歧化反应。
第2题
由附表六中查出酸性溶液中
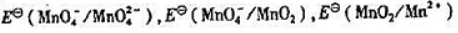
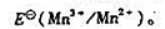
(1)颐出锰元素在酸性溶液中的元素电势图;
(2)计算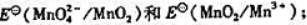
(3)MnO42-能否歧化?写出相应的反应方程式,并计算该反应的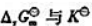 还有哪些物质能歧化?
还有哪些物质能歧化?
(4)计算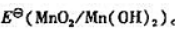
第3题
已知以下标准电极电势:

①画出酸性介质中铀的元素电势图;
②预测哪个氧化态最稳定;
③预测哪些氧化态会发生歧化反应;
④哪些氧化态在空气中不稳定?
第4题
试根据汞的元素电势图回答问题:
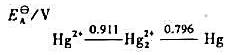
①在酸性介质中Hg22+能否发生歧化反应?
②计算反应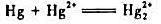 的平衡常数Kθ;
的平衡常数Kθ;
③拟使Hg(I)歧化为Hg(II)和Hg,应该怎样做?试举两个实例加以说明。
第5题
查表写出下列电极反应的标准电极电势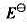 据此回答下列问题:
据此回答下列问题:
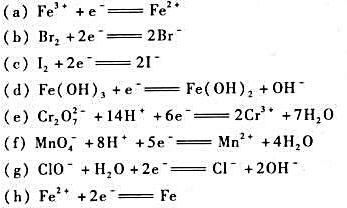
(1)哪些电极反应的电极电势值不受介质的酸碱性影响?
(2)哪种物质是酸性介质中最强的氧化剂?哪种物质是碱性介质中最强的还原剂?
(3)在标准状态下,哪些物质可以将Br-氧化?
(4)在标准状态下,哪些物质可以将Fe3+还原?
(5)降低pH,哪些电极反应的电极电势值升高?
第6题
在酸性溶液中,Mn的元素电势图为:
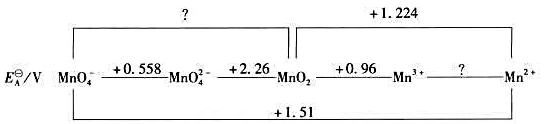
(1)计算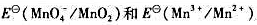 ;
;
(2)Mn的哪几种氧化态在酸性条件下不稳定易歧化?
第7题
由电极电势表查得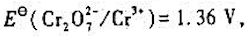 (1)K2Cr2O7在酸性介质中可以氧化上述电对中的哪种物质?写出有关反应方程式;
(1)K2Cr2O7在酸性介质中可以氧化上述电对中的哪种物质?写出有关反应方程式;
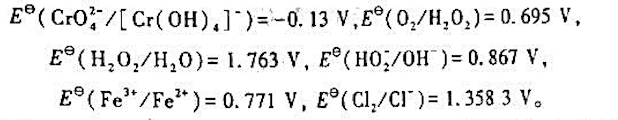
(2)欲使[ Cr(OH)4]-在碱性介质中被氧化,选择哪种氧化剂为好?写出有关反应方程式;
(3) K2Cr2O7, 在1 mol·L-1HCI溶液中能否将CI-氧化?为什么?若在12 mol·L-1HCI溶液中,反应能否进行?通过计算说明。
第8题
如图所示,已知:
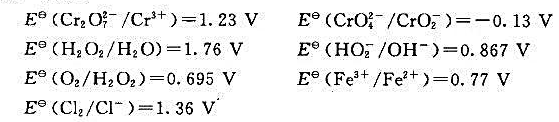
(1)试指出在酸性介质中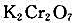 能氧化上面给出的哪些物质,并写出相关反应方程式。
能氧化上面给出的哪些物质,并写出相关反应方程式。
(2)欲使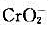 在碱性介质中被氧化,试指出上面给出的哪种氧化剂为好,并写出相关反应方程式。
在碱性介质中被氧化,试指出上面给出的哪种氧化剂为好,并写出相关反应方程式。
(3)试通过计算说明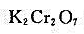 能否氧化浓度分别为
能否氧化浓度分别为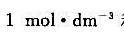 和
和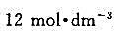 盐酸中的CI-。
盐酸中的CI-。
第9题
根据下面pH=1的酸性介质中Bi的元素电势图:

(2)作出Bi元素的自由能一氧化数图。
第10题
已知锰的元素电势图:

(1)求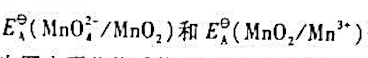 值;
值;
(2)指出图中哪些物质能发生歧化反应?
(3)指出金属Mn溶于稀HCI或H2SO4中的产物是Mn2+还是Mn3+,为什么?

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
