 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知300K时: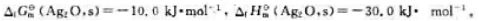
(1)试通过计算说明在300K、标准状态下、Ag2O(s)能否发生如下分解反应:
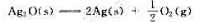
(2)计算在标准状态下Ag2O(s)发生分解反应的最低温度。
 更多“已知300K时: (1)试通过计算说明在300K、标准状态下、Ag2O(s)能否发生如下分解反应: (2”相关的问题
更多“已知300K时: (1)试通过计算说明在300K、标准状态下、Ag2O(s)能否发生如下分解反应: (2”相关的问题
第1题
300K、标准状态下,化学反应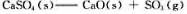 的标准摩尔焓变
的标准摩尔焓变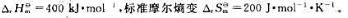
(1)在300K、标准状态下,上述反应能否自发进行?
(2)计算在标准状态下使上述反应自发进行的最低温度。
第2题
已知气体l2相邻振动能级的能量差Δɛ=0.426X10-20J;试求300K时1分子的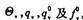 .
.
第3题
已知反应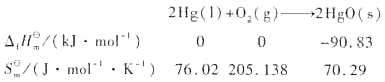
(1)通过计算说明在298. 15 K,标准态下反应能否自发进行?
(2)试估算反应自发进行的温度范围;
(3)试计算温度为900 K时反应的 (忽略反应的
(忽略反应的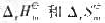 随温度的变化) ,并判断900 K时反应能否自发进行。
随温度的变化) ,并判断900 K时反应能否自发进行。
第4题
向电压VD1;(2)ID2=0.1mA时的正向电压VD2;(3)相应于ID1/VD2=10时的VD1/VD2值,并进行分析.
第5题
300K时,反应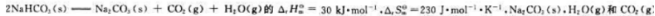 的标准摩尔生成吉布斯自由能AGR分别为-1044kJ·mol-1,-228kJ·mol-1和-393kJ·mol-1.试计算300K时NaHCO3(s)的标准摩尔生成吉布斯自由能.
的标准摩尔生成吉布斯自由能AGR分别为-1044kJ·mol-1,-228kJ·mol-1和-393kJ·mol-1.试计算300K时NaHCO3(s)的标准摩尔生成吉布斯自由能.
第6题
106J,请计算反应的Qp和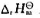 (WC,s,300K),已知C和w在300 K时的标准摩尔燃烧熔分别为-393.5kJ·mol-1和-837.5kJ·mol-1。
(WC,s,300K),已知C和w在300 K时的标准摩尔燃烧熔分别为-393.5kJ·mol-1和-837.5kJ·mol-1。
第7题
已知300时,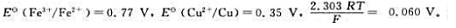 则可逆反应:
则可逆反应: 在300K时的标准平衡常数为()
在300K时的标准平衡常数为()
A、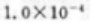
B、
C、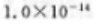
D、
第8题
已知NO分子在300K时的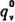 =1.0001,计算NO分子振动基态的分布数no与总分子数N之比
=1.0001,计算NO分子振动基态的分布数no与总分子数N之比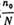 =(),结果说明().
=(),结果说明().
第9题
已知298.15K时,

(1)试确定298.15K时在标准状态下Co3+在水溶液中能否稳定存在;
(2)试确定298.15K时[Co(NH3)6]2+在1.0mol·L-1NH3溶液能否稳定存在(O2的压力为100kPa.其他有关离子浓度均为1.0mol·L-1),
第10题
298K时,已知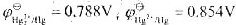 ,试计算(1)反应Hg2++e→1/2Hg22+的标准电极电势。(2)为反应Hg+Hg2+→Hg2-设计电池,并计算该反应的标准平衡常数。
,试计算(1)反应Hg2++e→1/2Hg22+的标准电极电势。(2)为反应Hg+Hg2+→Hg2-设计电池,并计算该反应的标准平衡常数。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
