 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知反应:

在45℃时,将0.0030mol的N2O.注入容积为0.50L的真空容器中,系统达平衡时,压力为26.3kPa,试计算:
(1)45℃时N2O4,的分解率及反应的标准平衡常数:
(2)25℃时反应的标准平衡常数;
(3)25℃时反应的标准摩尔熵变;
(4)反应的标准摩尔Cibbs函数变随温度变化的函数关系式.
 更多“已知反应:在45℃时,将0.0030mol的N2O.注入容积为0.50L的真空容器中,系统达平衡时,压力为26”相关的问题
更多“已知反应:在45℃时,将0.0030mol的N2O.注入容积为0.50L的真空容器中,系统达平衡时,压力为26”相关的问题
第1题
已知反应 在密闭容器内,当反应达到平衡后,若向系统内加Cl2(g),平衡()移动;升高温度,平衡()等容条件下加入惰性气体,平衡()移动;在移动。若加入催化剂,平衡()移动。
在密闭容器内,当反应达到平衡后,若向系统内加Cl2(g),平衡()移动;升高温度,平衡()等容条件下加入惰性气体,平衡()移动;在移动。若加入催化剂,平衡()移动。
第2题
反应: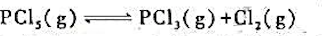 (1)523K时,将0.70mol的PCI5注入容积为2.0L的密闭容器中,平衡时有0.50molPCI5被分解了。试计算该温度下的平衡常数
(1)523K时,将0.70mol的PCI5注入容积为2.0L的密闭容器中,平衡时有0.50molPCI5被分解了。试计算该温度下的平衡常数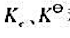 和PCI5的分解百分数。
和PCI5的分解百分数。
(2)若在上述容器中已达平衡后,再加入0.10 mol CI2则PCI, 5的分解百分数与朱加Cl2时相比有何不同?
(3)如开始时注入0.70 mol PCI5的同时,注入了0.10 mol Cl2.则平衡时PCI5的分解百分数又是多少?比较(2)(3) 所得结果,可得出什么结论?
第3题
.66kPa.
(1)当放人NH4CI时容器内已有压力为39.99kPa的HCl(g),求平衡时容器中的压力;
(2)容器内原有压力为6.666kPa的NH3(g),问需加多大压力的HCI,才能形成NH4CI.
(3)在520K时将0.02molNH4CI(s)和0.02molNH3引人到42.7升的抽空容器中,求平衡后各物质的量.
第4题
力p1=104.7kPa.在同样条件下,若将NH4I(s)放人抽真空的容器中,发生分解反应:NH4I(s) NH3(g)+HI(g),平衡时压力p2=18.9kPa.若将NH4C1(s)与NH4I(s)同时放人抽空容器中加热到613K,计算以上两个分解反应都达到平衡时,系统的总压.
NH3(g)+HI(g),平衡时压力p2=18.9kPa.若将NH4C1(s)与NH4I(s)同时放人抽空容器中加热到613K,计算以上两个分解反应都达到平衡时,系统的总压.
第5题
已知反应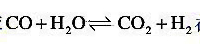 在700K时的平衡常数Kp=9,反应开始时系统中含有H2O、CO2、H2各1kmol,试求平衡组成.
在700K时的平衡常数Kp=9,反应开始时系统中含有H2O、CO2、H2各1kmol,试求平衡组成.
第6题
A、0.27
B、0.05
C、0.20
D、0.17
第7题
在400K时将纯NH4HCO3固体置于一抽空的密闭容器内,发生下列化学反应: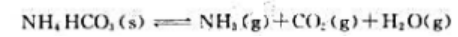 达到平衡时,测得容器内的总压力为akPa.则该反应在400K时的标准平衡数
达到平衡时,测得容器内的总压力为akPa.则该反应在400K时的标准平衡数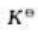 为()。
为()。
A、
B、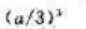
C、
D、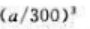
第8题
时间内压力保持在94.0kPa,后因HI(g)逐渐分解成H2(g)和I2(g),压力不断变化,计算容器内气体的最终平衡压力.已知403℃时,纯HI(g)的离解度为21.5%.假设达平衡时,容器内仍有NH4I(s),气体服从理想气体状态方程.
第9题
可逆反应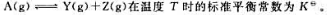 在此温度下当A的解离度为50%时,反应在密闭容器中达到化学平衡,此时系统的总压力p为()。
在此温度下当A的解离度为50%时,反应在密闭容器中达到化学平衡,此时系统的总压力p为()。
A、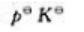
B、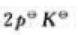
C、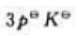
D、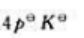
第10题
6.66kPa.
(1)当放入NH4HS(s)时容器内已有39.99kPa的H2S(g),求平衡时容器中的压力;
(2)容器内原有6.666kPa的NH3(g),问H2S压力为多大时才能形成NH4HS(s)?

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
