 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列说法是否正确?
(1)电池正极所发生的反应是氧化反应;
(2)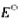 值越大则电对中氧化态物质的氧化能力越强;
值越大则电对中氧化态物质的氧化能力越强;
(3)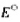 值越小则电对中还原态物质的还原能力越弱;
值越小则电对中还原态物质的还原能力越弱;
(4)电对中氧化态物质的氧化能力越强,则还原态物质的还原能力越强。
 更多“下列说法是否正确?(1)电池正极所发生的反应是氧化反应;(2)值越大则电对中氧化态物质的氧化能”相关的问题
更多“下列说法是否正确?(1)电池正极所发生的反应是氧化反应;(2)值越大则电对中氧化态物质的氧化能”相关的问题
第1题
A.在氧化还原反应中,若两个电对φθ值相差越大,则反应进行得越快
B.由于φθ(Fe2+/Fe)=-0.441V,φθ(Fe3+/Fe2+)=0.771V,故Fe3+与Fe2+能发生氧化还原反应
C.某物质的电极电势代数值越小,说明它的还原性越强
D.φθ值越大则电对中氧化型物质的氧化能力越强
第2题
A.电极反应中,增加氧化态物质的浓度。原电池的电动势降低
B. 代数值较小的电对的氧化态物质也有可能轧化
代数值较小的电对的氧化态物质也有可能轧化 代数值较大的电对中的还原态物质
代数值较大的电对中的还原态物质
C.原电池的电动势越大,电池反应的反应速率越快
D.氧化还原反应进行的方向是氧化能力较强的氧化型物质氧化还原能力较弱的还原型物质
第3题
A、歧化反应是同种物质内两种元素之间发生的氧化还原反应
B、歧化反应是同种物质内同种元素之间发生的氧化还原反应
C、歧化反应是两种物质中同种元素之间发生的氧化还原反应
D、歧化反应是两种物质中两种元素之间发生的氧化还原反应
第6题
在氧化还原反应中,凡是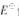 值小的氧化态一定不能氧化
值小的氧化态一定不能氧化 值大的还原态。()
值大的还原态。()
此题为判断题(对,错)。
第7题
如将下列氧化还原反应装配成原电池,试以电池符号表示之。
(1)
(2)
(3)
(4)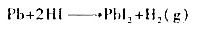
第8题
如果将下列氧化还原反应装配成电池,试用符号表示所组成的原电池。
(1)Zn(s)+2Ag+(aq)=Zn2+(aq)+2Ag(s)
(2)Cu(S)+FeCl3(aq)=CuCl(aq)+FeCl2(aq)
(3)Sn2+(aq)+2Fe3+(aq)=Sn4+(ag)+2Fe2+(aq)
(4)Zn(s)+2HCI(aq)=ZnCl2(a)+H2(g)
(5)MnO4-(0.1mol•dm-3)+8H+(10-4mol•dm-3)+5Fe2+(0.1mol•dm-3)=
Mn2+(0.1mol•dm-3)+5Fe(0.1mol•dm-3)+4H2O(l)
分析:首先根据反应方程确定电池的正负极,即发生氧化反应的电对为负极,发生还原反应的为正极,然后按照电池符号的书写规则写出即可。
第9题
分别写出下列各物质中指定元素的氧化数:
(1)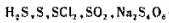 中硫的氧化数;
中硫的氧化数;
(2)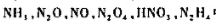 ,中氮的氧化数。
,中氮的氧化数。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
