 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列说法是否正确?为什么?举例说明.
(1)两个单键就组成一个双键.
(2)非极性分子中只有非极性键.
(3)极性分子中的化学键都有极性.
(4)有共价键的化合物都不可能形成离子晶体.
(5)全由共价键结合的物质只能形成分子晶体.
(6)分子量越大,分子间力越大.
(7)极性分子之间的作用力就是取向力.
(8)色散力仅存在于非极性分子之问.
(9)碘化氢的分子间力比碘化氢大,故碘化氢没有溴化氢稳定.
(10)氢键是一种特殊的分子间力,仅存在于分子之间.
 更多“下列说法是否正确?为什么?举例说明.(1)两个单键就组成一个双键.(2)非极性分子中只有非极性键.”相关的问题
更多“下列说法是否正确?为什么?举例说明.(1)两个单键就组成一个双键.(2)非极性分子中只有非极性键.”相关的问题
第1题
第2题
下列说法是否正确?为什么?
(1) s电子与s电子间形成的键是σ键,p电子与电子间形成的键是π键;
(2)直线形分子都是非极性分子,非直线形分子都是极性分子;
(3)相同原子间双键的键能是单键键能的两倍;
(4)用1s轨道与3p轨道混合形成4个sp3杂化轨道;
(5)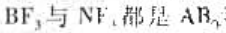 型分子,所以它们都是sp2杂化型,形成平面三角形分子
型分子,所以它们都是sp2杂化型,形成平面三角形分子
(10)凡是含氢的化合物,其分子间都能产生氢键。
第3题
A、由同种元素原子组成的双原子分子一定是非极性分子
B、由同种元素原子组成的多原了分子一定是非极性分子
C、由极性共价键形成的分子一定是极性分子
D、非极性分子中的化学键一定都是非极性键
第4题
A.在离子晶体中不可能存在非极性键
B.在共价化合物的分子晶体中不可能存在离子键
C.在极性分子中不可能存在非极性键
D.在原子晶体中不可能存在极性共价键
第7题
第10题

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
