 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
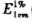 (245nm)=560]
(245nm)=560]
 更多“称取维生素C0.05g溶于100ml的0.005mol/L硫酸溶液中,再准确量此溶液2.00ml稀释至100ml,取此溶液”相关的问题
更多“称取维生素C0.05g溶于100ml的0.005mol/L硫酸溶液中,再准确量此溶液2.00ml稀释至100ml,取此溶液”相关的问题
第1题
已知维生素C的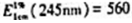 ,称取含维生素C的样品0.0500g溶于100mL的5.00×103mol·L-1硫酸溶液中,再准确量取此溶液2.00mL稀释至100.0mL,取此溶液于1.00cm吸收池中,在
,称取含维生素C的样品0.0500g溶于100mL的5.00×103mol·L-1硫酸溶液中,再准确量取此溶液2.00mL稀释至100.0mL,取此溶液于1.00cm吸收池中,在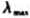 =245nm处測得A值为0.551,求样品中维生素C的质量分数。
=245nm处測得A值为0.551,求样品中维生素C的质量分数。
第2题
第3题
准确量取30.00ml弱酸HA,加水稀释至100ml,在下列电池中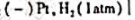
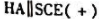 为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA溶液。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。(1)计算弱酸HA的Ka;(2)原弱酸HA的浓度是多少?(φSCE=0.242V)。
为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA溶液。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。(1)计算弱酸HA的Ka;(2)原弱酸HA的浓度是多少?(φSCE=0.242V)。
第4题
准确量取30.00ml弱酸,加水稀释至100ml。以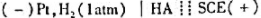 为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。φSCE=0.242V。计算:
(1)弱酸HA的Ka。
(2)原弱酸HA的浓度。
第5题
第6题
第7题
中,用待标定的NaOH溶液滴定至计量点,用去19.10ml.计算:

第8题
第9题
第10题
0.0mL比色管内用邻二氮菲显色,定容后在510nm处测得吸光度如下:

取1.00mL含Fe2+未知溶液稀释到100.00mL,再取稀释液5.00mL,在50.0mL比色管内用同样方法显色定容后测得吸光度A=0.47.求未知溶液中Fe2+的浓度.

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
