 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
如何解释下列事实:
(1)锂的电离能比铯大,但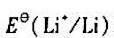 却比
却比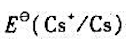 小;
小;
(2)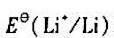 比
比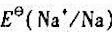 小,但锂同水的作用不如钠激烈;
小,但锂同水的作用不如钠激烈;
(3) LiI比KI易溶于水,而LiF比KF难溶于水;
(4) BeCl2 为共价化合物,而CaCl2为离子化合物;
(5)金属钙与盐酸反应剧烈,但与硫酸反应缓慢;
(6)消防队员的空气背包中放有KO2。
 更多“如何解释下列事实:(1)锂的电离能比铯大,但 却比 小;(2) 比 小,但锂同水的作用不如钠激烈;(3) L”相关的问题
更多“如何解释下列事实:(1)锂的电离能比铯大,但 却比 小;(2) 比 小,但锂同水的作用不如钠激烈;(3) L”相关的问题
第2题
第3题
解释如下现象:
(1)镀锡的铁,铁先腐蚀,镀锌的铁,锌先腐蚀。
(2)锂的电离势和升华热都比钠大,为什么锂的电极电势比钠更小(在金属活动顺序表中更远离氢)?
(3)铜和锌在元素周期系里是邻居,然而它们在金属活动顺序中的位置却相去甚远,试通过波恩-哈伯循环分析铜和锌的电极电势相差这么大主要是由什么能量项决定的。
(4)有人说,燃料电池是“一种通过燃烧反应使化学能直接转化为电能的装置”。这种说法正确吗?说明理由。燃料电池的理论效率有可能超过100%吗?燃料电池
(5)铁能置换铜而三氯化铁能溶解铜。
(6)ZnO22-{即Zn(OH)42-}的碱性溶液能把铜转化为Cu(OH)42-而把铜溶解。
(7)将MnSO4溶液滴入KMnO4酸性溶液得到MnO2沉淀。
(8)Cu+(aq)在水溶液中会歧化为Cu2+(aq)和铜。
(9)Cr2+(aq)在水溶液中不稳定,会与水反应。
(10)将C12水(溶液)滴入l-、Br-的混合溶液,相继得到的产物是l2、HlO3和Br2,而不是l2、Br2和HlO3。
第4题
第5题
第6题
请回答下列有关氮元素性质的问题:
(1)为什么N-N键的键能(167kJ.mol-1)比P-P键(201kJ.mol-1)的小?而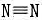 键的键能(942kJ.mol-1)又比
键的键能(942kJ.mol-1)又比 键(481kJ.Mol-1)的大?
键(481kJ.Mol-1)的大?
(2)为什么氮不能形成五卤化物?
(3)为什么N2的第一电离能比N原子的小?
第7题
第8题
简要回答下列问题:
(1)电解NaCl熔盐制取金属Na的过程中,为什么要加入CaCl2?由此带来的负面影响是什么?
(2)为什么金属Mg与冷水反应极慢,却可以迅速与热水或NH4Cl水溶液发生反应?
(3)什么是离子势φ?为什么φ的大小可以影响一些氧化物的水化物的解离方式?
(4)为什么加热MgCl2·6H2O时得不到无水盐?
(5)为降低煤炭燃烧时排向大气的SO2量,可以把CaO或CaCO3掺到含硫的煤炭中。试说明这种做法的化学原理,写出相关的化学反应方程式。
(6)Li+和Mg2+半径十分接近,试分析它们的碳酸盐分解温度的高低。
(7)锂的第一电离能比钠大,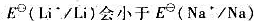 ?既然
?既然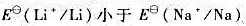 ,为什么锂与水的反应却不如钠剧烈?
,为什么锂与水的反应却不如钠剧烈?
(8)试说明锂的哪些性质与镁相似而有别于钠、钾。
(9)试说明铍的哪些性质与铝相似而有别于镁、钙。
(10)试用价层电子对互斥理论和杂化轨道理论,讨论XeF6分子的几何构型和中心原子的轨道杂化方式。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
