 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 更多“电池PtIH2(100kPa)IHCI(b=0.10mol Kg-1)ICl2(100kPa)IPt在25℃时电动势为1.4881V,试计算HCI溶液中HCI的平均离子活度因子。 ”相关的问题
更多“电池PtIH2(100kPa)IHCI(b=0.10mol Kg-1)ICl2(100kPa)IPt在25℃时电动势为1.4881V,试计算HCI溶液中HCI的平均离子活度因子。 ”相关的问题
第1题
自发电池: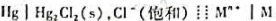 。在25℃时,测得电动势为0.100V,如将Mn+浓度稀释50倍,测得电池电动势为0.050V,此时金属离子的电荷数n是多少?
。在25℃时,测得电动势为0.100V,如将Mn+浓度稀释50倍,测得电池电动势为0.050V,此时金属离子的电荷数n是多少?
第2题
电池: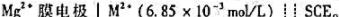 。在25℃时,测得电动势为0.387V。
。在25℃时,测得电动势为0.387V。
(1)当用未知溶液代替上述已知Mg2+溶液时。测得电池电动势为0.425V,求此溶液的pMg为多大?
(2)若溶液替代引起液接电位Ej的不稳定值为±1mV,则Mg2+浓度测定产生的相对误差有多大?波动范围为多少?
第5题
为了测定CuY2-的稳定常数,组成下列电池:
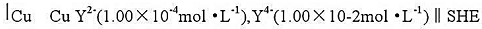
25℃时,测得电池电动势为0.227V,计算KcuY2-
第6题
25℃时,电池Pt|H2(pθ)|H2SO4(a=1)IAu3O3,Au的电动势E=I.362V.请:
(1)写出电极反应和电池反应:
(2)25℃时电池的标准电动势和反应的ΔtGm及Kθ;
(3)25℃时Au2O3的标准生成摩尔吉布斯丽数:
(4)25℃时Au与Au2O3平衡时O2的活度和压强.
已知H2O(l)的标准生成青布斯兩数ΔtGmθ(298K)=-236kJ·mol-1.
第7题
计算25°C时,下列电池的电动势,并标明电池的正负极。
已知: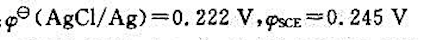
Ag,AgCl|NaCl(0.1mol•L^-1),NaF(0.001mol•L^-1)1LaFs单晶膜
|NaF(0.1mol•L^-1)|ISCE
第8题
电池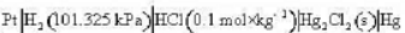 电动势召与温度T的关系为
电动势召与温度T的关系为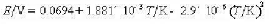
(1)写出电池反应:(2)计算25°C时该反应的DrCm.DrSm.DrHm以及电池恒温可逆放电时该反应过程的Qr.m
第9题
298K时,电池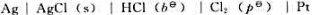 的电动势为1.1362v,电动势的温度系数为-5.95X10-4V·K-1.
的电动势为1.1362v,电动势的温度系数为-5.95X10-4V·K-1.
(1)写出电池反应;
(2)计算298K时该反应的 和标准平衡常数
和标准平衡常数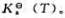
第10题
溶液适用Debye-Huckel极限公式.25℃时该电池电动势为0.5V.转移电子数为1时电池反应的摩尔反应焓为200kJ·mol-1,请:
(1)写出电极反应及电池反应;
(2)求25℃时,MCI的平均活度系数和电池的标准电动势:
(3)求此电池反应的ΔtGm、ΔtGmθ、ΔtSmθ和温度系数:
(4)求此电池在35℃时的电动势.
第11题

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
