 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
根据平衡移动原理,讨论下列反应:
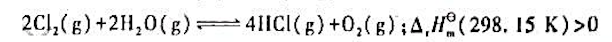
将Cl 2、H2O,HCI,O2四种气体混合后,反应达平衡时,若进行下列爷项操作,对平衡数值各有何影响(操作项目中没有注明的是指温度不变、体积不变)?
操作项目 平衡数值
(1)加O2 H2O的物质的量
(2)加O2 HCI的物质的址
(3)加O2 O2的物质的量
(4)增大容器的体积 H2O的物质的量
(5)减小行器的体积 Cl2的物质的量
(6)减小容器的体积 Cl2的分压
(7)减小行器的体积 (8)升高温度 (9)升高温度 HCI的分压;
(10)加催化剤 HCI的物貭的量;
 更多“根据平衡移动原理,讨论下列反应:将Cl 2、H2O,HCI,O2四种气体混合后,反应达平衡时,若进行下列爷”相关的问题
更多“根据平衡移动原理,讨论下列反应:将Cl 2、H2O,HCI,O2四种气体混合后,反应达平衡时,若进行下列爷”相关的问题
第1题
根据Le Chatelier原理,讨论下列反应:
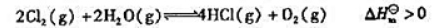
将Cl2,H2O(g),HCl(g),O2四种气休混合后,反应达到平衡时,下列左面的操作条件改变对右面各物理鼠的平衡数值有何影响(操作条件中没有注明的,是指温度不变和体积不变)?

第2题
已知反应 在密闭容器内,当反应达到平衡后,若向系统内加Cl2(g),平衡()移动;升高温度,平衡()等容条件下加入惰性气体,平衡()移动;在移动。若加入催化剂,平衡()移动。
在密闭容器内,当反应达到平衡后,若向系统内加Cl2(g),平衡()移动;升高温度,平衡()等容条件下加入惰性气体,平衡()移动;在移动。若加入催化剂,平衡()移动。
第3题
在600℃,100kPa时下列反应达到平衡:
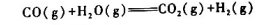
现在把压力提高到5×104kPa,问:
(1)若各气体均视为理想气体,平衡是否移动?
(2)若各气体的逸度因子分别为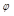 (CO2)=1.09,
(CO2)=1.09,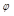 (H2)=1.10,
(H2)=1.10,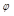 (CO)=1.20,
(CO)=1.20,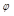 (H2O)=0.75,与理想气体反应相比,平衡向哪个方向移动?
(H2O)=0.75,与理想气体反应相比,平衡向哪个方向移动?
第4题
反应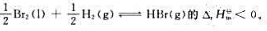 上述可逆反应达到化学平衡后,降低温度时,平衡()移动:缩小容器的体积增大压力时,平衡()加入催化剂时,标准平衡常数()移动;升高温度时,标准平衡常数()。
上述可逆反应达到化学平衡后,降低温度时,平衡()移动:缩小容器的体积增大压力时,平衡()加入催化剂时,标准平衡常数()移动;升高温度时,标准平衡常数()。
第5题
向下列各平衡体系加入一定量不参与反应的气体,并保持总体积不变,平衡将如何
移动?为什么?
①CO(g)+H2O(g)=CO2(g)+H2(g)
②4NH3(g)+7O2(g)=4NO2(g)+6H2O(g)
③SbCl3(g)=SbCl3(g)+Cl2(g)
第6题
可逆反应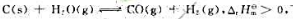 下列说法正确的是().
下列说法正确的是().
A、达到平衡时反应物和生成物的分压相等
B、降低温度有利平衡向正反应方向移动
C、升高温度有利于平衡向正反应方向移动
D、增大压力对平衡没有影响
第7题
一定条件下反应2NO(g)+O2(g) 2NO2(g)达到平衡.已知该反应的
2NO2(g)达到平衡.已知该反应的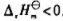 .若保持温度不变、增大压力,则平衡();若保持温度、体积不变,加入惰性组分,则平衡();若保持压力不变、降低温度,则平衡().(选择填入:向左移动、向右移动、不发生移动.)
.若保持温度不变、增大压力,则平衡();若保持温度、体积不变,加入惰性组分,则平衡();若保持压力不变、降低温度,则平衡().(选择填入:向左移动、向右移动、不发生移动.)
第8题
反应N2(g)+3H2(g)=2NH3(g)(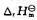 >0)达到平衡后采取下列哪种方法能使平衡向有移动。()
>0)达到平衡后采取下列哪种方法能使平衡向有移动。()
A.加入催化剂
B.降低温度
C.增加H2的压力
D.降低系统的总压
第9题
反应 在某温度下达到平衡。
在某温度下达到平衡。
(1)若其他条件不变,加入催化剂是否会引起平衡移动?
(2)若增大任一反应物或生成物的分压,化学平衡向哪一方向移动?
(3)升高温度时标准平衡常数是否发生变化?化学平衡向哪一方向移动?
(4)缩小容器的体积增大压力时,化学平衡向哪一方向移动?标准平衡常数是否发生变化?
第10题
可逆反应 达到平衡后,升高温度,平衡向正反应方向移动。这说明()
达到平衡后,升高温度,平衡向正反应方向移动。这说明()
A、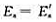
B、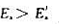
C、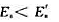
D、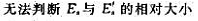

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
