 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.sp杂化轨道中
B.sp2 杂化轨道中
C.sp3 杂化轨道中
D.p轨道中
 更多“吡咯分子中氮原子上的电子对处于”相关的问题
更多“吡咯分子中氮原子上的电子对处于”相关的问题
第1题
A、中心原子采取sp3杂化轨道成键的分子,其空间构型一定是四面体
B、CH,分子中的sp3杂化轨道是由H原子的1s轨道和C原子的2p轨道组合而成
C、CH分子中的sp3杂化轨道是由C原了的1s轨道和2p轨道组合而成
D、Sp杂化轨道是由中心原子的最外层s轨道和最外层1个p轨道组合面成
第2题
A.sp 杂化轨道
B.sp 2 杂化轨道
C.sp 3 杂化轨道
D.都一样
第3题
A、杂化轨道是由不同原子的价层能量相近的原子轨道组合而成
B、有几个原子轨道参加杂化,就形成几个杂化轨道
C、杂化轨道比杂化前的原子轨道成键能力强
D、不同类型的杂化轨道间的夹角不同
第4题
臭氧O2的键角为116.8°。若用杂化轨道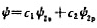 描述中心氧原子的成键轨道,试按键角与轨道成分的关系式
描述中心氧原子的成键轨道,试按键角与轨道成分的关系式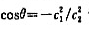 计算:
计算:
(1)成键杂化轨道ψ中系数c1和c2值;
(2)成键杂化轨道的每个原子轨道贡献的百分数。
第5题
A.N2分子包含一个s键和两个π键
B.CO分子中存在配位键
C.原子形成共价键时必须遵守饱和性和方向性原则
D.sp2杂化轨道是由1s和2p轨道杂化而成
第6题
A、参加杂化的各原子轨道中必须有电子存在
B、原子轨道杂化后形成的轨道数目比杂化前更多
C、原子轨道杂化后形成成键能力更强的原子轨道
D、中心原子在形成分子是所采取的的杂化方式宗师相同的

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
